شباهت های ریشه ای چند بیماری با وجود تفاوت های ظاهری آنها
آیا این شباهت ها میتواند درمانی ریشه ای و موثر را برای این بیماری ها پیدا کند؟
ای ال اس ALS و دمانس، پیوندهای مولکولی مشترکی دارند!
22 مارس 2024
خلاصه:اسکلروز جانبی آمیوتروفیک (ALS) و دژنراسیون لوبار فرونتومپورال (FTLD) با وجود تظاهرات بالینی متفاوت، ویژگیهای سلولی و مولکولی بسیار مشابهی دارند.
این مطالعه، بیان RNA را در بیش از 620000 سلول از قشر حرکتی و جلوی مغز 73 اهداکننده، مورد تجزیه و تحلیل قرار داد و تغییرات تقریباً یکسانی را در بیان ژن در آسیبپذیرترین نورونها در هر دو بیماری نشان داد.
این، نشان می دهد اهداف درمانی بالقوه برای ALS، ممکن است برای FTLD و برعکس درمان های دمانس بر ای ال اس موثر باشد.
به علاوه، این مطالعه شباهت هایی را در اشکال ارثی و پراکنده sporadic این اختلالات پیدا کرد که به فرآیندهای مولکولی مشترک در پایین دست، اشاره دارد.
این تحقیق، راههای جدیدی را برای درک و درمان بیماریهای عصبی باز میکند و بر نیاز به مطالعه ی ژنها در گونهها و رفتارهای مختلف تأکید میکند.
حقایق کلیدی:
مطالعهای که توسط محققان MIT و کلینیک مایو انجام شد، نشان داد اسکلروز جانبی آمیوتروفیک (ALS) و دژنراسیون لوبار فرونتومپورال (FTLD) ویژگیهای سلولی و مولکولی بسیار مشابهی دارند، با وجود اینکه بر مناطق مختلف مغز تأثیر میگذارند و علائم بالینی متفاوتی را نشان میدهند.
این تحقیق بیان RNA را در بیش از 620000 سلول از قشر حرکتی و جلوی مغز، تجزیه و تحلیل کرد و تغییرات ژنی تقریباً یکسانی را در آسیبپذیرترین نورونهای بیماری کشف کرد و این، مسیرهای مولکولی مشترکی را نشان میدهد.
این کشف به اهداف درمانی بالقوه ای اشاره می کند که می تواند بر هر دو بیماری ALS و FTLD موثر باشد و اهمیت درک زیربنای مولکولی مشترک این بیماری های عصبی را برجسته می کند.
در ظاهر، اختلال حرکتی اسکلروز جانبی آمیوتروفیک (ALS) که به عنوان بیماری لو گریگ هم شناخته میشود، و اختلال شناختی دژنراسیون لوبار پیشانی گیجگاهی (FTLD)- که زمینه ساز زوال عقل فرونتوتمپورال است- به روشهای بسیار متفاوتی ظاهر میشوند. علاوه بر این، شناخته شده است که آنها عمدتاً مناطق بسیار متفاوتی از مغز را تحت تأثیر قرار می دهند.
با این حال، پزشکان و دانشمندان در طول سالها به چندین شباهت اشاره کردهاند.
یک مطالعه جدید درمجله یCellنشان میدهد که این بیماریها همپوشانیهای قابلتوجهی در سطوح سلولی و مولکولی دارند و اهداف بالقوهای را نشان میدهند. این اهداف میتوانند درمانهای قابل استفاده برای هر دو اختلال را به همراه داشته باشند.
با نگاهی فراتر از نورونها، این مطالعه تفاوتهای بیان ژن را در بسیاری از انواع دیگر سلولهای مغزی مشخص کرد.
مقاله ی جدید به رهبری دانشمندان MIT و کلینیک مایو، الگوهای بیان RNA را در 620000 سلول شامل 44 نوع سلول مختلف در سراسر قشر حرکتی و قشر جلوی مغز از نمونههای مغزی پس از مرگ 73 اهداکننده با تشخیص ALS، FTLD یا افرادی که از نظر عصبی سالم بودند، ردیابی کرد.
مانولیس کلیس نویسنده ارشد مقاله و استاد آزمایشگاه علوم کامپیوتر و هوش مصنوعی در MIT، گفت: «ما روی دو ناحیه ی مغز تمرکز کردیم که انتظار داشتیم بین این دو اختلال تأثیر متفاوتی بگذارد.
به نظر می رسد در سطح مولکولی و سلولی، تغییراتی که ما پیدا کردیم در این دو اختلال تقریباً یکسان باشد و بر زیرمجموعه های تقریباً یکسانی از انواع سلول بین دو منطقه تأثیر بگذارد.
در واقع، یکی از برجستهترین یافتههای این مطالعه، نشان داد در هر دو بیماری، آسیبپذیرترین نورونها در ژنهایی که بیان میکنند و هم در نحوه تغییر بیان این ژنها در هر بیماری تقریباً یکسان هستند.
میریام هیمن، استادیار مؤسسه ی یادگیری و حافظه Picower و دپارتمان علوم مغز و شناختی در MIT، میگوید: «این شباهتها کاملاً چشمگیر بود. این نشان میدهد که درمان ALS ممکن است برای FTLD و برعکس اعمال شود.
مطالعه ی ما می تواند به هدایت برنامه های درمانی ای کمک کند که احتمالا بر هر دو بیماری موثر است.
هیمن و کلیس با نویسنده ی ارشد ورونیک بلزیل، استادیار علوم اعصاب در کلینیک مایو در فلوریدا، که اکنون مدیر مرکز تحقیقات ALS در دانشگاه واندربیلت است، همکاری کردند.
یکی دیگر از دستاوردهای کلیدی مطالعه این است که اهداکنندگان مغز با اشکال ارثی یا پراکنده این بیماری، تغییرات مشابهی در بیان ژن تغییر یافته، نشان دادند، حتی اگر قبلاً تصور میشد این تغییرات دلایل متفاوتی دارند.
دکتر سید سلمان فاطمی . نورولوژیست, [03/22/2024 10:27 ب.ظ]
این، نشان میدهد فرآیندهای مولکولی مشابه در پاییندست، ممکن است منشأ بیماریها باشد.
کلیس گفت: «شباهت مولکولی بین فرم خانوادگی (تکژنیک) و اشکال پراکنده (چند ژنیک) این اختلالات نشان میدهد علل مختلف در مسیرهای مشترک بیماری زا، همگرا میشوند.
این امر پیامدهای مهمی هم برای درک ناهمگنی بیماری ها و هم برای درک اختلالات پیچیده و نادر دارد.»
نمایههای عملا غیرقابل تشخیص
این همپوشانی به ویژه هنگام بررسی سلولهای آسیبدیده، مشهود بود. در ALS که باعث فلج پیشرونده و در نهایت مرگ می شود، سلول های در معرض خطر در مغز، نورون های حرکتی بالایی (UMN) در لایه ی 5 قشر حرکتی است.
همزمان، در نوع رفتاری دمانس فرونتوتامپورال (bvFTD)، شایع ترین نوع FTLD- که با تغییرات شخصیت و رفتار مشخص می شود- آسیب پذیرترین نورون ها نورون های دوکی یا سلول های فون اکونومو von Economo cells هستند که در لایه ی 5 نواحی پیشانی مغز، یافت می شود.
مطالعه ی جدید نشان میدهد در حالی که سلولها در زیر میکروسکوپ، متفاوت به نظر میرسند و اتصالات مشخص و متمایزی را در مدارهای مغزی ایجاد میکنند، بیان ژن آنها در سلامت و بیماری، به طرز چشمگیری مشابه است.
سباستین پیندا، نویسنده ی اصلی این مطالعه، همراه با یک دانشجوی فارغ التحصیل که به طور مشترک توسط هیمن و کلیس نظارت می شدند، گفتند: UMN ها و نورون های دوکی، هیچ شباهتی به هم ندارند و در مناطق بسیار متفاوتی از سیستم عصبی سکونت دارند.
قابل توجه بود که دیدیم آنها در سطح مولکولی عملاً غیرقابل تشخیص به نظر می رسند و بسیار شبیه بیماری پاسخ می دهند.
محققان دریافتند بسیاری از ژنهای دخیل در این دو بیماری، مژکهای اولیه ی مشابهی را عرضه کردند.
این مژکها ساختارهای آنتنمانند کوچکی روی سطح سلول هستند که تغییرات شیمیایی در محیط اطراف سلول را حس میکنند.
این مژک ها برای هدایت رشد آکسون ها یا رشته های عصبی بلندی که نورون ها برای اتصال به نورون های دیگر میگستراند، ضروری هستند. سلولهایی که بیشتر به این فرآیند وابسته هستند، معمولاً آنهایی هستند که طولانیترین زائده ها را دارند و به نظر میرسد در هر دو بیماری، آسیبپذیرتر هستند.
این تجزیه و تحلیل همچنین نشان داد نوع دیگری از نورون ها- که ژنSCN4Bرا به مقدار زیاد بیان می کند و قبلاً با هیچ یک از این بیماری ها مرتبط نبوده است- بسیاری از این ویژگی های مشابه را دارد و اختلالات مشابهی را نشان می دهد.
هیمن گفت: «ممکن است تغییرات در این جمعیت سلولی با مشخصه ی ضعیف، زمینه ساز پدیدههای مختلف بیماری بالینی مرتبط باشد.
این مطالعه همچنین نشان داد آسیبپذیرترین سلولها ژنهایی را بیان میکنند که از نظر ژنتیکی با هر کدام از این دو بیماری مرتبط است، و یک مبنای مکانیکی محتمل برای برخی از این ارتباطات ژنتیکی فراهم میکند. هیمن گفت که این الگو همیشه در شرایط نورودژنراتیو صدق نمی کند.
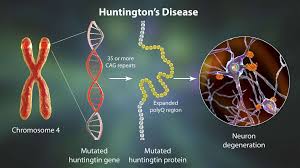
به عنوان مثال، بیماری هانتینگتون توسط یک جهش شناخته شده در ژن هانتینگتین ایجاد میشود، اما نورونهایی که به شدت تحت تأثیر قرار گرفتهاند، بیش از سایر سلولها هانتینگتین یا ژن بیماری هانتینگتون را درگیر نمیکند و همین امر در مورد برخی از ژنهای مرتبط با بیماری آلزایمر هم صادق است.
با نگاهی فراتر از نورونها، این مطالعه تفاوتهای بیان ژن را در بسیاری از انواع دیگر سلولهای مغزی مشخص کرد.
قابل توجه اینکه محققان چندین نشانه ی چالش را در سیستم گردش خون مغزی، مشاهده کردند.
سد خونی مغزی (BBB) یک سیستم فیلتری است که به شدت تنظیم میکند کدام مولکولها میتوانند از طریق رگهای خونی به مغز بروند یا از آن خارج شوند. اعتقاد بر این است که این سد در هر دو اختلال، آسیب میبیند.

محققان با تکیه بر توصیف قبلی خود از عروق مغزی انسان و تغییرات آن در بیماری هانتینگتون و آلزایمر توسط هیمن، کلیس و همکارانش از جمله لی-هوی تسای، مدیر موسسه Picower، فهمیدند پروتئین های مورد نیاز در حفظ یکپارچگی رگ های خونی در تخریب عصبی، کاهش می یابد یا در جای خود قرار نمی گیرد.
آنها همچنین کاهش HLA-E را دیدند و این، مولکولی است که تصور می شود از تخریب BBB توسط سیستم ایمنی جلوگیری می کند.
با توجه به شباهت های مولکولی و مکانیکی فراوان در ALS و FTLD، هیمن و کلیس گفتند کنجکاو هستند چرا برخی از بیماران با ALS و برخی دیگر با FTLD و برخی دیگر با هر دو اما با ترتیبی متفاوت، مراجعه می کنند.
در حالی که مطالعه ی حاضر نورونهای حرکتی فوقانی مغز را مورد بررسی قرار میدهد، هیمن و کلیس اکنون به دنبال شناسایی نورونهای حرکتی پایینتر در نخاع هستند.
کلیس میگوید: «تحلیلهای تک سلولی ما بسیاری از مسیرهای بیولوژیکی مشترک را در ALS، FTLD، هانتینگتون، آلزایمر، زوال عقل عروقی، زوال عقل لوی بادی و چندین اختلال عصبی نادر دیگر نشان دادهاند.
این نشانههای متداول میتواند مسیر را برای یک رویکرد مدولار جدید در درمان دقیق و مشخص این بیماری ها هموار کند و میتواند بینشها و امیدهای جدید مورد نیاز را به ارمغان آورد.
https://neurosciencenews.com/als-ftd-molecular-neuroscience-25796/
آدرس مطب : اصفهان ، خیابان آمادگاه ، روبروی داروخانه سپاهان ، مجتمع اطبا ، طبقه اول
تلفن : 32223328 - 031