پیر شدن، فرایندی حتمی یا قابل برعکس شدن است؟
بررسی های ژنتیکی و مولکلولی، از بدن انسان، پایگاهی برای اهداف ژن، ترسیم میکند.
در حقیقت بدن، ساخته میشود تا به عنوان سرزمینی در اشغال ژن(مستعمره ی ژنتیکی) مورد بهره برداری قرار بگیرد تا ساختار ژنتیکی، به هدف خود برسد. در این نگاه، بدن و تغییرات آن از جمله پیری تدریجی، اصیل نیست بلکه راهکارهایی برای تحقق اهداف ساختار ژنهاست.
قدرت انسان در سالهای اخیر در بررسی ژنها و پروتئین ها و توانایی ایجاد دگرگونی در آن، دریچه ی جدیدی است که راه را برای تغییر در پایگاه و مستعمره ی ژنها- که مورد استفاده هستند تا نقشه ی حیات به اهداف خود برسد- هموار میسازد.
اکنون راه هموار شده است تا به جای دستکاری بدن، ریشه و نقشه ی بدن یعنی ساختار ژنتیکی و پروتئین ها دستکاری شود.
این ساختار ژنتیکی خودش تابع ریشه ها و اصول دیگری است ولی در ساختار بدن موجودات زنده، ژن ساختاری بنیادین و اصیل، به حساب می آید.
بدن هایی- که پایگاه یا مستعمره های برای اهداف ژنهاست- با تغییر اهداف فرمانده یعنی ساختار ژنتیکی، به سادگی قابل تغییر خواهد بود و بسیاری از غیر ممکن ها با این مداخله ها ممکن میشود.
12 آوریل 2023
مطالعات پیری در پنج حیوان، نشان می دهد که چگونه می توان کاهش زوال را معکوس کرد!
به نظر می رسد صاف کردن دست اندازهای سرعت گیر در یک مسیر سلولی مهم، در افزایش سن نقش دارد.
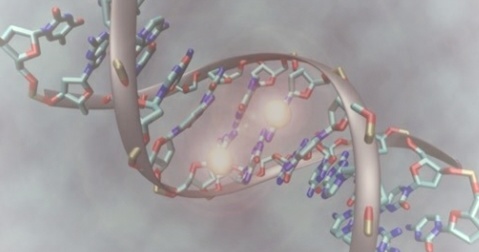
آر ان ای پلیمراز RNAپلیمراز (آبی)، DNA (بنفش) را باز می کند و از آن به عنوان یک الگو برای تولید رشته ای از RNA پیام رسان(قرمز) استفاده می کند.
در سلول های پیر، این روند تسریع می شود.
طبق مطالعهای- که در 12 آوریل در مجله ی Nature منتشر شد- به نظر میرسد پیری فرآیندهای سلولی را در پنج نوع بسیار متفاوت زندگی در انسان، مگس میوه، موش، موش و کرم، تحت تأثیر قرار میدهد.
این یافتهها میتواند به توضیح عواملی که باعث پیری میشود و پیشنهادهایی برای چگونگی معکوس کردن آن کمک کند.
لیندسی وو، بیوشیمیست در UNSW سیدنی استرالیا، میگوید: «این یک حوزه واقعاً بنیادین و جدید برای درک چگونگی و چرایی پیری است.
با افزایش سن حیوانات، انواع فرآیندهای مولکولی درون سلولها کمتر قابل اعتماد میشوند؛ جهشهای ژنی بیشتر و انتهای کروموزومها جدا و کوتاهتر میشوند.
آندریاس بایر، زیستشناس محاسباتی در دانشگاه کلن آلمان، میگوید: بسیاری از مطالعات اثرات پیری را بر بیان ژن مورد بررسی قرار دادهاند، اما تعداد کمی از آنها بررسی کردهاند که چگونه رونویسی تحت تأثیر قرار میگیرد - فرآیندی که در آن اطلاعات ژنتیکی از یک رشته DNA طرحواره به مولکولهای RNA کپی میشود.
کپی بی دقت:
برای پی بردن به این موضوع، بایر و همکارانش تغییرات رونویسی گسترده ژنومی را در سنین مختلف بالغین، در پنج موجود زنده مورد تجزیه و تحلیل قرار دادند: کرم نماتد، مگس میوه، موش، موش صحرایی و انسان.
محققان اندازهگیری کردند که پیری چگونه سرعت حرکت آنزیمی- که رونویسی را انجام میدهد یعنی RNA پلیمراز II (Pol II)- را در طول رشته DNA هنگام کپی کردن RNA تغییر میدهد.
آنها دریافتند که به طور متوسط، Pol II با افزایش سن، سریعتر می شود، اما در هر پنج گروه، دقت آن کمتر و بیشتر مستعد خطا می شود. Beyer میگوید: «ما شاهد عدم تطابق بیشتری بین خواندهها و ژنوم مرجع بودیم.
تحقیقات قبلی نشان داده بود که محدود کردن رژیم غذایی و مهار سیگنالدهی انسولین، میتواند پیری را در بسیاری از حیوانات به تاخیر بیندازد و طول عمر را افزایش دهد. محققان سپس بررسی کردند که آیا این اقدامات، بر سرعت Pol II تأثیری دارد یا نه. در کرمها، موشها و مگسهای میوه- که دارای جهش در ژنهای سیگنالدهنده انسولین بودند- Pol II با سرعت کمتری حرکت کرد. این آنزیم همچنین در موش هایی که رژیم غذایی کم کالری داشتند، کندتر حرکت می کرد.
اما سوال نهایی این بود که آیا تغییرات در سرعت Pol II بر طول عمر تاثیر می گذارد یا نه. Beyer و تیمش بقای مگسهای میوه و کرمهای حامل جهشی را- که سرعت Pol II را کاهش میداد- پیگیری کردند. این حیوانات 10 تا 20 درصد بیشتر از همتایان غیر جهش یافته ی خود، عمر کردند.
هنگامی که محققان از ویرایش ژن برای معکوس کردن جهش در کرم ها استفاده کردند، طول عمر حیوانات کوتاه شد. Beyer میگوید: «این واقعاً یک ارتباط علی ایجاد کرد.
بالا بردن سرعت:
محققان متعجب بودند که آیا شتاب Pol II را میتوان با تغییرات ساختاری در نحوه بستهبندی DNA درون سلولها توضیح داد. برای به حداقل رساندن فضایی که اشغال میکنند، رشتههای وسیعی از اطلاعات ژنتیکی در اطراف پروتئینهایی به نام هیستونها به بستههایی به نام نوکلئوزوم، پیچیده میشوند. با تجزیه و تحلیل سلولهای ریه ی انسان و سلولهای ورید ناف، محققان دریافتند که سلولهای پیر، حاوی نوکلئوزومهای کمتری هستند و مسیر Pol II را برای حرکت سریعتر، هموار میکنند. هنگامی که تیم بایر، هیستون ها را در سلول ها تقویت کرد، Pol II با سرعت کمتری حرکت کرد. در مگسهای میوه، سطوح بالای هیستون به نظر میرسید که طول عمر آنها را افزایش دهد.
کالین سلمان، که پیری پستانداران را در دانشگاه گلاسکو، بریتانیا مطالعه میکند میگوید: این مطالعه «یک کار واقعاً هیجانانگیز» است که نشان میدهد چگونه مکانیسمهای پیری در گونههای مرتبط با هم سازگار است. همچنین راه را هموار میکند تا کشف شود چگونه Pol II می تواند هدفی برای داروهایی باشد که روند پیری را کند می کنند. تغییرات در فرآیند رونویسی Pol II در بسیاری از بیماریها، از جمله انواع مختلف سرطان نقش دارد، و طیف وسیعی از داروها ساخته شدهاند که Pol II و مولکولهای تسهیل کننده ی آن را، هدف قرار میدهند.
سلمان میگوید: «ممکن است فرصتهایی برای استفاده ی مجدد از برخی از این داروها در بررسی اثرات آنها بر پیری وجود داشته باشد.
doi: https://doi.org/10.1038/d41586-023-01040-x
منابع
Debès, C. et al. Nature https://doi.org/10.1038/s41586-023-05922-y (2023).
https://www.nature.com/articles/d41586-023-01040-x...
برخی توضیحات دکتر سلمان فاطمی نورولوژیست در ایران
آدرس مطب : اصفهان ، خیابان آمادگاه ، روبروی داروخانه سپاهان ، مجتمع اطبا ، طبقه اول
تلفن : 32223328 - 031