درمان های جدید سرطان
دستکاری مصنوعی سلول های سیستم ایمنی
سیستم ایمنی بدن انسان طی میلیون ها سال تکامل، برای مقابله با عوامل مهاجم، بسیار پیشرفته شده است ولی تغییرات سریع از جمله تغییر شرایط آب و هوایی، ورود ویروس و باکتری و یا قارچ جدید و یا آلودگی هوا می تواند باعث یک رویارویی ناموفق از طرف سیستم ایمنی شود.
حتی واکسن های جدید با تغییر سیستم ایمنی، هرچند بدن را در برابر یک گونه ی بیماری زا مجهز می کند، میتواند در دراز مدت، سیستم ایمنی پیچیده و قدرتمند انسان را در مواجهه با شرایط و عوامل بیماری زا و سلولهای جهش یافته ی جدید، ناتوان کند.
در این شرایط، دست انسان بسته نیست. پیشرفت های علمی و تکنولوژیک انسان امروز به خصوص در زمینه ی دستکاری های ژنتیکی و دستکاری سلول ها میتواند او را مجهز کند.
بررسی تفصیلی یکی از این روش های نوین در درمان سرطان:
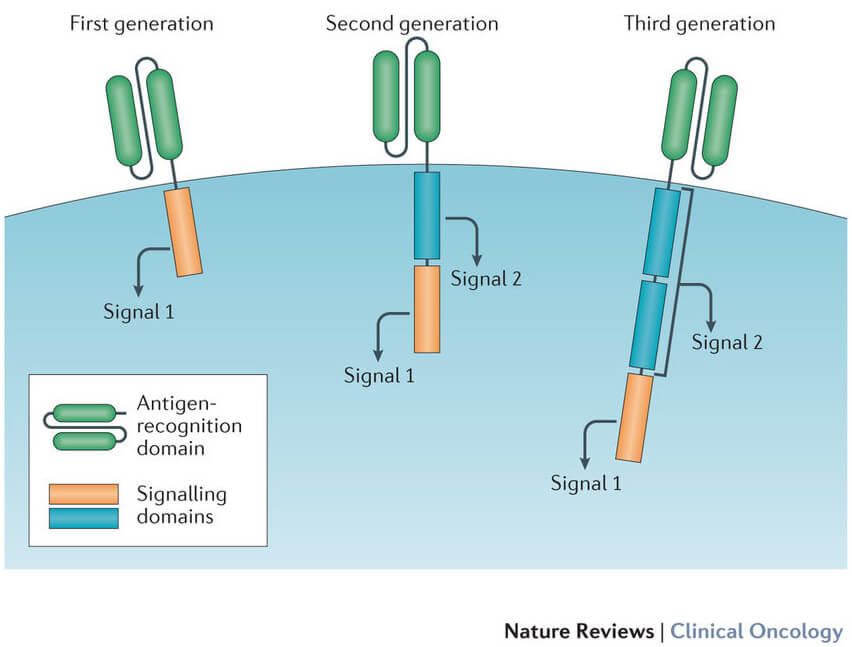
سلول های CAR T: مهندسی سلول های ایمنی بیماران برای درمان سرطان آنها
حوزههای پیام دهی همتحریکی Co-stimulatory signaling domains، به نسلهای جدیدتر سلولهای کار تی CAR T اضافه شدهاند تا توانایی آنها را در تولید سلولهای T بیشتر، پس از تزریق و زنده ماندن طولانیتر این سلولهای تی در گردش خون بهبود بخشند.
راندن سلول های CAR T به جلو. Nat Rev Clin Oncol. 2016 13, 370-383.
برای چندین دهه، پایه های درمان سرطان، جراحی، شیمی درمانی و پرتودرمانی بوده است. اینها همچنان پایه های اصلی درمان هستند، اما دسته بندی های جدید درمان اخیراً به تغییر تصویر درمان برای افراد مبتلا به سرطان کمک کرده است.
دهه ی 2000، نشانه ظهور درمانهای هدفمندی مانند ایماتینیب (گلیوک) و تراستوزوماب (هرسپتین) بود.
اینها داروها سلولهای سرطانی را با تغییرات مولکولی خاص- که عمدتاً در این سلولها دیده میشود- پیدا میکند و از بین میبرد.
ده ها درمان هدفمند اکنون درمان های استاندارد برای بسیاری از سرطان ها هستند و در طول دهه گذشته، ایمونوتراپی یعنی درمانی- که قدرت سیستم ایمنی بیمار را برای حمله به تومورها به کار می گیرد و تقویت می کند- به سرعت به درمان موثر تبدیل شده است و بسیاری آن را ستون پنجم درمان سرطان می نامند زیرا داروهای تقویت کننده ی سیستم ایمنی توانایی کوچک کردن و حتی ریشه کن کردن تومورها را در برخی از افراد مبتلا به سرطان پیشرفته، نشان داده است.
در درصد کمی از بیماران، این پاسخ های درمانی می تواند سال ها ادامه داشته باشد.
به عنوان مثال، داروهایی به نام مهارکنندههای شناختی در ایمنی، در حال حاضر برای درمان افراد مبتلا به انواع سرطان از جمله ملانوم، ریه، کلیه، مثانه و لنفوم استفاده گستردهای دارند.
شکل دیگری از ایمونوتراپی به نام CAR T-cell therapy، هیجان قابل توجهی را در میان محققان و انکولوژیست ها ایجاد کرده است. اگرچه درمانهای CAR chimeric antigen receptor T-cell بهاندازه مهارکنندههای ایست بازرسی ایمنی به طور گسترده مورد استفاده قرار نمیگیرند، اما همان توانایی را در ریشهکن کردن لوسمیها و لنفومهای بسیار پیشرفته و جلوگیری از سرطان، نشان دادهاند.
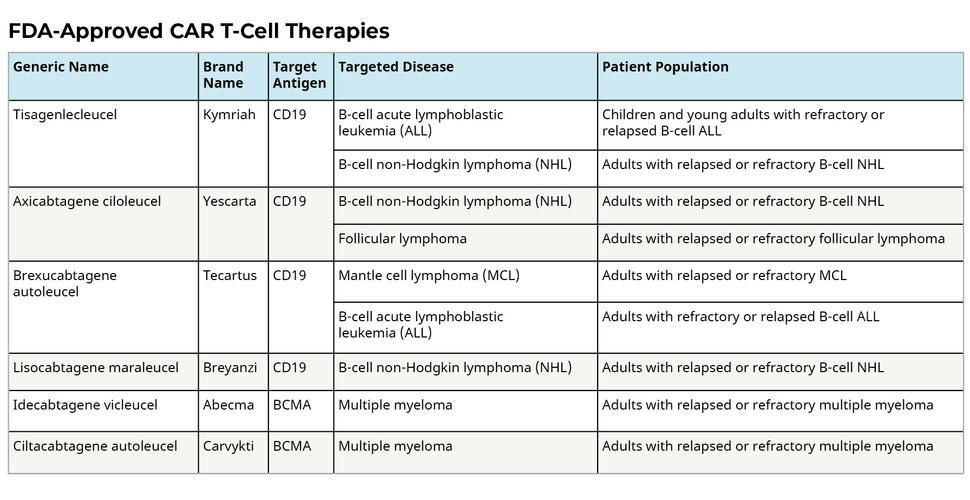
از سال 2017، شش درمان با سلول T CAR، توسط سازمان غذا و داروی آمریکا (FDA) تایید شده است. همه ی آنها برای درمان سرطان های خون، از جمله لنفوم، برخی از انواع لوسمی، و اخیرا، مولتیپل میلوما تایید شده اند.
علیرغم هیجانی که در اطراف این درمان ها وجود دارد، در تعداد کمی منجر به بقای طولانی مدت می شود. در مورد بیش از نیمی از بیمارانی- که تحت درمان قرار گرفتند- به دلیل هزینه درمان انتقاد وجود دارد. این هزینه در مورد جدیدترین درمان با سلول T CAR بیش از 450000 دلار است.
استیون روزنبرگ، MD، Ph.D.، رئیس شعبه جراحی در مرکز تحقیقات سرطان NCI (CCR)، گفت: با این وجود، پس از سالها تحقیق پرزحمت، درمانهای سلول T CAR وارد جریان اصلی درمان سرطان شدهاند. پیشگام درمان با سلول T CAR
دکتر روزنبرگ، گفت: «[سلولهای CAR T] اکنون به طور گسترده در ایالات متحده و سایر کشورها در دسترس است و به یک درمان استاندارد برای بیماران مبتلا به لنفوم تهاجمی تبدیل شدهاند.» آنها به بخشی از پزشکی مدرن تبدیل شدهاند.
درمان با سلول T CAR: یک داروی زنده
Renier J. Brentjens، MD، Ph.D.
از مرکز سرطان Memorial Sloan Kettering در نیویورک، یکی دیگر از رهبران در زمینه سلول های T CAR توضیح میدهد که سلول های CAR T معادل «دادن داروی زنده به بیماران» است.
همانطور که از نام آنها پیداست، سلولهای T - که به تنظیم پاسخ ایمنی کمک میکنند و مستقیماً سلولهای آلوده به پاتوژنها را از بین میبرند - ستون درمان با سلولهای T CAR هستند.
درمانهای سلول T در حال حاضر برای هر بیمار، شخصی سازی شده است. این سلولهای نوآوری شده، با جمع آوری سلول های T از بیمار و مهندسی مجدد آنها در آزمایشگاه برای تولید پروتئین هایی به نام گیرنده های آنتی ژن CAR ساخته می شوند. CARها پروتئین ها یا آنتی ژن های خاصی را در سطح سلول های سرطانی تشخیص می دهند و به آن متصل می شوند.
کارل جون، MD، از مرکز سرطان آبرامسون دانشگاه پنسیلوانیا، یکی دیگر از رهبران در زمینه سلول درمانی، توضیح داد که این گیرنده ها مولکول های مصنوعی هستند، آنها به طور طبیعی وجود ندارند.
پس از اینکه سلولهای T بازسازیشده به میلیونها عدد در آزمایشگاه گسترش می یابند، دوباره به بیمار تزریق میشوند. اگر همه چیز طبق برنامه پیش برود، سلول های CAR T به تکثیر در بدن بیمار ادامه می دهند و با راهنمایی گیرنده مهندسی شده ی خود، سلول های سرطانی را- که آنتی ژن هدف را روی سطوح خود نگه می دارند- شناسایی میکند و می کشد.
درمانهای CAR T-cell که تا به امروز توسط FDA تأیید شدهاند، یکی از دو آنتی ژن CD19 یا BCMA را روی سلولهای B، هدف قرار میدهند.
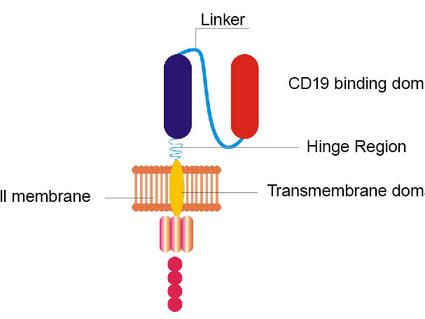
ساخت CAR T Cell:
تعداد فزاینده ای از درمان های CAR T-cell در حال توسعه و آزمایش در مطالعات بالینی هستند. اگرچه تفاوتهای مهمی بین هر درمان خاص وجود دارد که میتواند بر عملکرد آن در بیماران تأثیر بگذارد، اما همه ی آنها اجزای مشابهی دارند.
هر chimeric antigen receptor CAR غشای سلولی را پل می زند. بخشی از گیرنده، خارج از سلول و بخشی در داخل سلول قرار دارد.
بخشی از CAR که بیرون از سطح سلول است معمولاً از قطعات یا حوزه هایی از آنتی بادی های ساخته شده در آزمایشگاه تشکیل شده است. اینکه کدام دامنه استفاده می شود بر میزان تشخیص یا اتصال گیرنده به آنتی ژن روی سلول های تومور، تأثیر می گذارد. بخش داخلی هر CAR دارای دامنه های پیامرسانی و تحریک کننده است و این سیگنال ها را پس از تعامل گیرنده با آنتی ژن به سلول منتقل می کند. دامنه های مختلفی- که استفاده می شود- می تواند بر عملکرد کلی سلول ها تأثیر بگذارد.
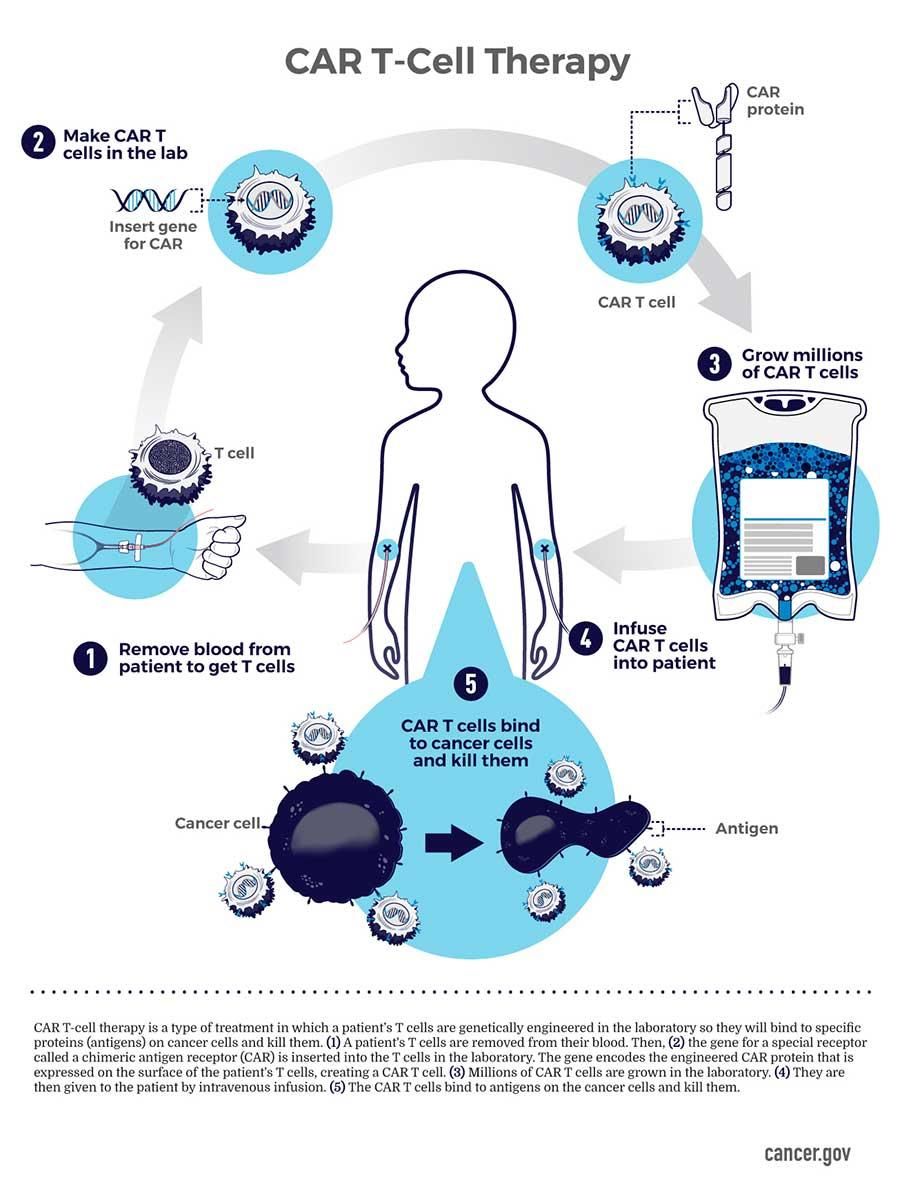
گزینه های درمانی جدید:
توسعه ی اولیه ی درمانهای CAR T-cell عمدتاً بر شایعترین سرطان در کودکان، لوسمی حاد لنفوبلاستیک (ALL) متمرکز بود.
بیش از 80 درصد کودکانی- که در آنها ALL در سلولهای B ایجاد میشود- با شیمیدرمانی شدید درمان میشوند. اما درمانهای مؤثر برای بیمارانی که سرطانشان پس از شیمیدرمانی یا پیوند سلولهای بنیادی عود میکند، محدود شده است.
درمان دوم CAR T-Cell برای لنفوم تایید شده است
یک گزینه جدید برای برخی از بیماران مبتلا به لنفوم شایع است.
با این حال، در سال 2017، با تایید FDA ،
tisagenlecleucel (Kymriah)
به عنوان گزینه جدید درمانی مطرح شد. این بر اساس آزمایشهای بالینی است که نشان میدهد این درمان میتواند سرطان را در کودکان مبتلا به ALL عودکننده، ریشه کن کند.
در برخی موارد، درمان با سلول T CAR، به اندازه کافی مورد مطالعه قرار گرفته است و جزئیات در مورد پیامدهای بلندمدت در کودکان در حال آشکار شدن است.
به عنوان مثال، یک تیم تحقیقاتی تحت رهبری NCI، اخیراً در مورد پیگیری طولانی مدت از کودکان مبتلا به ALL عود کننده- که تحت درمان با سلول های CAR T به عنوان بخشی از یک کارآزمایی بالینی قرار گرفته بودند- گزارشی ارائه دادند.
از کودکانی که پیوند سلول های بنیادی بالقوه درمانی را دریافت کردند، تقریباً 60 درصد از آنها، 5 سال بعد هنوز زنده بودند بدون اینکه سرطان آنها عود کند یا کودکان هیچ مشکل مرتبط با بیماری را تجربه کنند.
تری فرای، MD، که چندین آزمایش بالینی برای درمان سلولهای CAR-T را در NCI و اخیراً در بیمارستان کودکان کلرادو رهبری کرده است، گفت: پیشرفتهای حاصل شده در درمان با سلولهای T-CAR در کودکان مبتلا به ALL «خیلی خوب بوده است».
دکتر فرای ادامه داد از آنجا که درمان با سلول T CAR به طور گسترده در دسترس قرار گرفته است، به سرعت به استاندارد مراقبت برای کودکان مبتلا به ALL عودکننده، تبدیل شده است.
سلولهای CAR T که در آنها CD19 قرار گرفته است، به بزرگسالان و کودکان مبتلا به لنفوم تهاجمی پیشرفته، امید میدهند.
جیمز کوچندرفر، MD، از مرکز تحقیقات سرطان NCI، که چندین کارآزمایی از درمانهای سلولهای T CAR را در بیماران مبتلا به سلولهای B منتشر کرده است، گفت: قبل از توسعه ی سلولهای CAR T، بسیاری از این بیماران «عملاً غیرقابل درمان بودند».
دکتر کوچندرفر گفت: نتایج در لنفوم تا به امروز به شکلی باورنکردنی، موفقیت آمیز بوده است، و سلول های CAR T تبدیل به یک درمان پرکاربرد برای چندین نوع لنفوم شده است.
دکتر سید سلمان فاطمی . نورولوژیست, [01/02/2024 06:51 ب.ظ]
مدیریت عوارض جانبی درمان های CAR T-cell
مانند تمام درمانهای سرطان، درمان سلول T CAR میتواند عوارض جانبی شدیدی از جمله مرگ انبوه سلولهای B تولیدکننده ی آنتیبادی و عفونتها ایجاد کند. یکی از شایع ترین و جدی ترین عوارض جانبی، سندرم انتشار سیتوکین (CRS) است.
سلول های T به عنوان بخشی از وظایف مربوط به ایمنی، سیتوکین ها را آزاد می کنند. سیتوکین ها پیام رسان های شیمیایی هستند که به تحریک و هدایت پاسخ ایمنی کمک می کنند. در مورد CRS، سلولهای T تزریق شده، سیتوکینها را به جریان خون میرسانند و باعث عوارض جانبی جدی، از جمله تب شدید و افت فشار خون میشوند.
در برخی موارد، CRS شدید می تواند کشنده باشد با این حال حضور این سندرم، نشان می دهد که سلول های T در بدن کار می کنند.
دکتر کوچندرفر توضیح میدهد که به طور کلی، بیمارانی که بیشترین میزان سرطان را در بدن خود دارند، بیشتر احتمال دارد که CRS شدید ناشی از سلول های CAR T را تجربه کنند.
در بسیاری از بیماران، چه کودکان و چه بزرگسالان، اشکال خفیف CRS را می توان با درمان های حمایتی استاندارد، از جمله استروئیدها، مدیریت کرد. و همانطور که محققان تجربه بیشتری در مورد درمان با سلول T CAR به دست آورده اند، راه هایی را برای مدیریت بهتر موارد جدی تر CRS کشف کرده اند.
بخش بزرگی از این مدیریت، داروی توسیلیزوماب (Actemra) است. این دارو که در درجه ی اول، برای درمان بیماریهای التهابی مانند آرتریت نوجوانان استفاده میشود، فعالیت IL-6 را مسدود میکند. این اینترلوکین، سیتوکینی است که اغلب در مقادیر زیادی توسط سلولهای T و ماکروفاژها ترشح میشود.
دیگر عارضه جانبی که در درمانهای CAR T-cell مورد توجه قرار میگیرد، اثرات عصبی، از جمله گیجی شدید، فعالیت شبه تشنج و اختلال در گفتار است. علت دقیق این عوارض جانبی عصبی (که به نام سندرم سمیت عصبی مرتبط با سلول مؤثر ایمنی یا immune effector cellassociated neurotoxicity syndrome ICANS هم شناخته میشود) هنوز نامشخص است.
اگرچه توسیلیزوماب برای درمان CRS موثر است، اما به نظر نمی رسد که توسیلیزوماب به ICANS کمک کند.
جنیفر برودن، MD، که در چندین کارآزمایی درمانهای CAR T-cell در مرکز سرطان NCI شرکت دارد، توضیح میدهد که استروئیدها در حال حاضر بهترین گزینه درمانی برای ICANS شدید هستند، به ویژه دگزامتازون- که بهتر از سایر استروئیدها در سیستم عصبی مرکزی نفوذ میکند.
درمان با سلول T بازسازی شده CAR عوارض جانبی کمتری ایجاد می کند
برای افراد مبتلا به لنفوم، درمان ایمن تر، به اندازه طراحی اصلی سلول T CAR موثر است.
دکتر برودنو گفت که راه های مختلف پیشگیری از CRS و ICANS در حال حاضر تحت مطالعه هستند. یک رویکرد، استفاده پیشگیرانه از توسیلیزوماب و استروئیدهای با دوز پایین است. او گفت، اگرچه مطالعات بیشتری مورد نیاز است، داده ها تا کنون اطمینان بخش هستند.
درمان های دیگر برای ICANS در حال بررسی است. به عنوان مثال، مطالعات کوچکتر نشان داده است که Anakinra (Kineret)- که برای درمان آرتریت روماتوئید استفاده می شود- ممکن است به پیشگیری از ICANS شدید در بیماران تحت درمان با سلول های T-CAR کمک کند.
دکتر برودونو توضیح میدهد که یک ایده دیگر برای محافظت در برابر CRS و ICANS شدید، این است که خود سلولهای کارتی را اصلاح کنیم.
به عنوان مثال، در یک کارآزمایی بالینی کوچک بر روی بزرگسالان مبتلا به لنفوم، بیمارانی که تحت درمان با یک سلول CAR T هدفمند، با CD-19 بازسازی شده توسعه یافته در NCI، قرار گرفتند، عوارض جانبی عصبی شدید کمتری نسبت به شکل اولیه همان CAR داشتند.
آنتی ژن های هدف بیشتر، از جمله برای تومورهای جامد
تحقیقات روی سلولهای CAR T با سرعتی سریع ادامه دارد، از جمله صدها آزمایش بالینی در حال انجام است. بخشی از این گسترش، محصول کار محققانی است که آنتی ژن های اضافی را روی سلول های تومور شناسایی کرده اند. این آنتی ژن ها ممکن است اهداف خوبی برای سلول های CAR T باشند.
اگرچه CD19 و BCMA تنها آنتی ژن هایی هستند که برای آنها درمان های CAR T مورد تایید FDA وجود دارد، درمان هایی از CAR T-cell توسعه یافته اند که آنتی ژن های دیگر را- که معمولا در سرطان های خون یافت می شوند- هدف قرار می دهند؛ از جمله درمان هایی که چندین آنتی ژن را در یک زمان مورد هدف قرار می دهند.
اما در مورد استفاده از سلول های CAR T برای درمان تومورهای جامد، مانند سرطان مغز، سینه یا کلیه چه می شود؟
در این زمینه پیشرفت ها به سختی به دست آمده است. دکتر روزنبرگ گفت تلاشها برای شناسایی آنتیژنهایی که روی سطح تومورهای جامد هستند اما سلولهای سالم نیستند، تا حد زیادی ناموفق بوده است.
غلبه بر فرسودگی سلول T در ایمونوتراپی
دکتر سید سلمان فاطمی . نورولوژیست, [01/02/2024 06:51 ب.ظ]
هدف قرار دادن پروتئین های دخیل در فرسودگی سلول های T، ممکن است ایمونوتراپی را تقویت کند.
یکی دیگر از موانع تومورهای جامد، محیط اطراف آنها است. به عنوان مثال، موانع فیزیکی می توانند از رسیدن سلول های CAR T تزریق شده به سلول های تومور جلوگیری کنند. سایر اجزای ریزمحیط، مانند مولکولهای سرکوبکننده سیستم ایمنی تولید شده توسط سلولهای تومور یا سایر سلولهای ایمنی، میتوانند باعث اختلال در عملکرد سلولهای CAR T شوند و آنها را قادر به انجام وظایف خود یعنی کشتن سلولی نکنند.
دکتر کریستال مکال، مدیر موسسه پارکر برای ایمونوتراپی سرطان در دانشگاه استنفورد، گفت: شاید بزرگترین مانع، یک مشکل قدیمی است: ناهمگنی تومور .
به عبارت دیگر، تومورهای جامد از یک نوع سرطان می توانند از نظر مولکولی کاملاً از بیمار به بیمار و حتی در یک بیمار خاص متفاوت باشند. به عنوان مثال، ممکن است هیچ آنتی ژن قابل هدف گیری روی برخی از سلول های تومور وجود نداشته باشد، یا شاید وجود داشته باشد، اما به اندازه کافی برای سلول های CAR T وجود نداشته باشد تا آنطور که باید عمل کند.
با وجود این موانع، محققان به تلاش برای یافتن راه هایی برای استفاده از سلول های CAR T برای درمان تومورهای جامد ادامه می دهند.
یک رویکرد، شامل تلاش برای گول زدن محیط سرکوب کننده سیستم ایمنی بسیاری از تومورهای جامد است. برای مثال، چندین گروه تحقیقاتی سلولهای CAR T زرهدار را توسعه دادهاند که می تواند با ترشح سیتوکین های خاص و مولکول های دیگر در ریزمحیط دشوار، حرکت کند.
سایر محققان با تکیه بر فناوریهای استاندارد مهندسی CAR و هدف قرار دادن یک آنتی ژن سطحی واحد روی سلولهای سرطانی، رویکردهای مرسومتری را دنبال میکنند.
مطالعه CAR T-Cell نویدبخش سرطان دوران کودکی است
در مدل های موشی سرطان های رایج کودکان، درمان تومورها را کوچک یا ریشه کن کرده است.
برای مثال ، پس از نتایج امیدوارکننده از مطالعات آزمایشگاهی و مبتنی بر حیوانات، گروه دکتر مکال در استنفورد یک آزمایش بالینی با پشتیبانی NCI را از درمانهای سلولهای T CAR که پروتئینی را روی تومورهای جامد به نام B7-H3 هدف قرار میدهند، راهاندازی کردند.
در آزمایش دیگری، گروه او در حال بررسی یک درمان با سلول T CAR است که مولکولی را روی سلولهای سرطانی به نام GD2 در برخی از کودکان و بزرگسالان جوان مبتلا به سرطان مغزی کشنده به نام DIPG مورد هدف قرار میدهد.
دکتر مکال در نشست سالانه انجمن ایمونوتراپی سرطان در سال 2021 توضیح داد که برای آزمایش سلول T GD2 CAR، نحوه تصور اولیه و نحوه انجام آن، کاملاً متفاوت است.
در ابتدا، بیماران فقط با تزریق داخل وریدی اولیه سلول های CAR T درمان می شدند. اما نتایج حاصل از مطالعات مدل حیوانی یک درمان مشابه با CAR T-cell، محققان را به تغییر کارآزمایی سوق داد: به بیمارانی که به انفوزیون اولیه داخل وریدی پاسخ میدهند، دوزهای کوچکتری داده شد که مستقیماً به مغز وارد میشود.
او گزارش داد که توانایی دادن دوزهای متعدد به بیماران، منجر به بهبود وضعیت تومور (به عنوان مثال، کاهش اندازه تومور) و علائم مرتبط با سرطان آنها شده است.
تیم تحقیقاتی همچنین توانستند به سرعت تغییراتی در سلولهای GD2 CAR T مورد استفاده در آزمایش و نحوه تولید آنها انجام دهند تا کارایی و ایمنی بالقوه آنها را بهبود بخشند. دکتر مکال گفت توانایی ایجاد چنین تغییرات سریعی اهمیت حیاتی نوآوری مداوم با درمان های سلولی را برجسته می کند.
او گفت: «همه ما در این زمینه آگهیم که فقط نوک کوه یخ را در مورد آنچه میتوانیم در رابطه با مهندسی این سلولهای CAR T انجام دهیم، میخراشیم. برای بسیاری از رویکردهای نسل بعدی، مشکلاتی وجود دارد که [اثربخشی آنها] را در تومورهای جامد محدود میکند.»
هدف NCI افزایش کارآزماییهای بالینی درمان با سلولهای کار تی است
درمان های خارج از قفسه ی
CAR T-cell:
CRISPR، کشنده های طبیعی و mRNA
محققان همچنین شروع به تجدید نظر در مورد منبع سلول های ایمنی برای درمان با سلول های T CAR کرده اند؛ این کار با استفاده از سلول های T جمع آوری شده نه از بیماران، بلکه از اهداکنندگان سالم انجام میشود.
هدف: درمانهای سلول T CAR که بهجای تولید برای هر بیمار، فوراً برای استفاده در دسترس خواهد بود.
تمام درمانهای CAR T-cell تایید شده توسط FDA بر یک ویروس خلع سلاح شده برای رساندن ماده ژنتیکی به سلولهای T برای تولید CAR تکیه دارند. اما برای سلولهای CAR T- که اکنون در آزمایشهای بالینی کوچک آزمایش میشوند- از فناوریهای ویرایش ژن مانند TALON و CRISPR برای وادار کردن سلولهای T اهدایی در تولید CAR استفاده میشود.
سایر car Tcellهای خارج از قفسه نیز از نوع متفاوتی از سلول های ایمنی به نام سلول های کشنده طبیعی (NK) استفاده می کنند.
دکتر سید سلمان فاطمی . نورولوژیست, [01/02/2024 06:52 ب.ظ]
بسیاری از این تحقیقات هنوز در روزهای اولیه خود هستند، اما برخی از درمانهای سلولی CAR NK در حال حاضر در آزمایشهای بالینی کوچک آزمایش میشوند
و نه تنها منبع سلولهای T و نوع سلول ایمنی مورد بازنگری قرار میگیرد، بلکه در جایی که درمانها واقعاً ساخته میشوند نیز مورد بازنگری قرار میگیرند.
به عنوان مثال، چندین گروه تحقیقاتی از فناوری نانو و رویکردهای مبتنی بر mRNA استفاده می کنند که به سلول های CAR T اجازه می دهد در داخل بدن ایجاد شوند .
سلول های CAR T: گزینه درمانی خط دوم برای NHL؟
آزمایشات بالینی نشان می دهد که سلول های CAR T ممکن است موثرتر از درمان استاندارد باشند.
در بیشتر موارد، درمان با سلول T CAR تا زمانی که سرطان فرد پس از چندین درمان دیگر بدتر نشده باشد، مورد توجه قرار نمی گیرد. اما این دیدگاه، شروع به تغییر کرده است.
اخیراً، در دو کارآزمایی بالینی بزرگ، درمان با سلول T CAR موثرتر از درمان استاندارد برای بیماران مبتلا به لنفوم غیر هوچکین است که سرطان آنها پس از شیمیدرمانی اولیه یا خط اول بازگشته است.
این یافته باعث شد برخی از کارشناسان به این نتیجه برسند که برای این بیماران، درمان با سلول های T CAR به زودی می تواند جایگزین شیمی درمانی، به عنوان درمان خط دوم استاندارد شود.
دکتر فرای گفت، برای برخی از کودکان مبتلا به ALL، استفاده از سلولهای CAR T به این روش جذاب خواهد بود. وی به طور خاص به کودکانی اشاره کرد که در معرض خطر بالای بیماری هستند. بیماری این بیماران پس از شیمی درمانی اولیه که معمولاً برای حدود 2.5 سال انجام می شود، عود می کند.
در واقع، آزمایشهای بالینی کوچکی در مورد سلولهای CAR T در کودکان مبتلا به ALL که پاسخ مطلوبی به درمان اولیه شیمیدرمانی خود ندارند، در حال انجام است .
دکتر فرای برای بیمارانی که به خوب پاسخ می دهند، گفت: می توانند 2 سال دیگر از شیمی درمانی معاف شوند. فکر کردن در مورد آن شگفت انگیز است.
فراتر از سلولهای CAR T:
TIL و TCR
سلولهای CAR T در مورد درمانهای سلولی بیشترین توجه را به خود جلب کردهاند. اما انواع دیگر درمانهای سلولی نیز در آزمایشهای بالینی کوچک، از جمله در بیماران مبتلا به تومورهای جامد، امیدوارکننده بودهاند.
یک نوع، که به عنوان لنفوسیت های نفوذ کننده تومور (TILs) شناخته می شود، از سلول های ایمنی استفاده می کند که به محیط داخل و اطراف تومور نفوذ کرده اند. محققان NCI اولین کسانی بودند که از TIL برای درمان موفقیت آمیز بیماران مبتلا به سرطان پیشرفته استفاده کردند. این کار در ابتدا در ملانوما و بعداً در چندین سرطان دیگر از جمله سرطان دهانه رحم انجام شد. اخیراً، محققان NCI تکنیکی را برای شناسایی TIL ها توسعه داده اند که سلول های سرطانی را با جهش های خاص آن سرطان تشخیص می دهد و افرادی را که سرطان آنها بیشتر به درمان TIL پاسخ می دهند مشخص میکند.
نوع دیگر درمان سلولی شامل مهندسی سلول های T بیماران برای بیان گیرنده سلول T خاص (TCR) است.
برخلاف CARها که از بخشهایی از آنتیبادیهای مصنوعی استفاده میکنند که میتوانند آنتیژنهای خاص را فقط در سطح سلولها تشخیص دهند، TCRها از گیرندههای طبیعی استفاده میکنند. این گیرنده های طبیعی میتوانند آنتیژنهایی را- که درون سلولهای تومور هستند- تشخیص دهند.
تا به امروز، سلولهای TCR در بیماران مبتلا به انواع تومورهای جامد، آزمایش شدهاند و در ملانوم و سارکوم امیدوارکننده هستند.
https://www.cancer.gov/about-cancer/treatment/research/car-t-cells
آدرس مطب : اصفهان ، خیابان آمادگاه ، روبروی داروخانه سپاهان ، مجتمع اطبا ، طبقه اول
تلفن : 32223328 - 031